Techniques
Techniques
Les méthodes de génie génétique
Les premières plantes transgéniques ont été cultivées commercialement aux Etats-Unis il y a 20 ans. La culture s’est ensuite propagée au Canada et à plusieurs pays d'Amérique du Sud. La plupart des plantes transgéniques sont résistantes aux herbicides ou produisent une toxine qui tue les insectes nuisibles. La majorité d'entre elles sont le maïs, le colza, le soja et le coton. Le seul animal transgénique autorisé à la consommation est un saumon, distribué en Amérique du Nord.
Nouvelles techniques de modification génétique
Cisgénèse
Transgénèse
Nouvelles techniques de modification génétique
Les nouvelles techniques de génie génétique regroupent des procédés très divers. Actuellement, deux types de techniques ont accéléré et multiplié notre capacité d’intervention dans les génomes des êtres vivants. D’une part, les méthodes d’édition génomique sont utilisées pour modifier de manière permanente le matériel génétique des organismes vivants. D’autre part, l’interférence ARN réduit au silence l’expression de gènes "encombrants" sans forcément nécessiter une modification du génome. La plus utilisée est la technologie de l’édition génomique.
Ces techniques ont le potentiel de modifier en profondeur la physiologie des organismes et leur utilisation comportent des risques et des incertitudes qu'il convient d'étudier. Ceci principalement car le fonctionnement du génome est encore largement inconnu. Modifier l'inconnu, même de manière ciblée, revient à ne pas pouvoir prédire le résultat de nos modifications.
Édition génomique
L’édition génomique se réfère à diverses méthodes de biologie moléculaire qui sont utilisées afin de couper dans le matériel génétique et copier/coller de nouvelles séquences d’ADN à l’endroit de la coupure. Celle-ci est basée sur l’utilisation de ciseaux moléculaires, appelés nucléases programmables, qui coupent dans le génome et permettent, au travers du système de réparation de l’ADN des cellules, de muter, modifier et insérer des gènes existants ou entièrement synthétiques dans une multitude d’organismes végétaux et animaux et de passer outre la barrière des espèces. Par rapport aux méthodes conventionnelles, ces méthodes permettent une augmentation du nombre de changements fait au génome en une seule opération (multiplexing) et sont applicables à un nombre plus important d’organismes vivants.
Nucléases programmables
Les "nucléases programmables" sont des enzymes qui lisent une séquence cible de quelques paires de bases d’ADN dans le génome puis coupent à cet endroit comme des ciseaux. Les nucléases peuvent être programmées pour reconnaître une séquences choisies du génome. Les scientifiques peuvent donc choisir quel gène couper et « quelle longueur » couper dans le génome de l’organisme de leur choix.
Les nucléases provoquent une coupure des deux brins d'ADN qui déclenche à son tour un mécanisme de réparation cellulaire de l’ADN qui peut être de deux types. Le premier reconstitue presque sans erreur la séquence d’origine. Le deuxième « recolle » les brins en faisant des erreurs, soit par rajout ou supression de quelques lettres (les bases de l’ADN) ou alors de plus longues séquences. Il est difficile de contrôler quel mécanisme est utilisé, mais il est décisif pour les effets de la madification. Le mécanisme le plus utilisé par la cellule est celui qui commet des erreurs. Il est utilisé par les scientifiques pour muter ou inactiver les gènes. La séquence du gène coupé peut être inactivée en insérant ou en enlevant des bases individuelles ou remplacée par une autre séquence fonctionnelle (p. ex. un autre gène). Plusieurs types de nucléases sont utilisés avec des précisions et des effets secondaires divers.
L'interférence à ARN
L'interférence à ARN est un processus cellulaire endogène, c’est-à-dire qu’il existe de manière naturelle dans toutes les cellules, dans lequel des molécules d'ARN sont utilisées pour bloquer l’expression des gènes de manière ciblée et donc empêcher la synthèse de la protéine correspodnante. C'est le mécanisme utilisé par les cellule pour réguler l'expression des gènes en fonction de l'environnement et des besoins. Ce mécanismes est extrêmement complexe puisque des milliers de gènes sont régulés à chaque seconde. Ce procédé est utilisé en biotechnologie pour produire des pesticides et des plantes génétiquement modifiées aux caractères divers (par exemple une pomme qui ne produit pas une certaine substance par exemple).
Ces fragments d’ARN peuvent être :1) synthétisés directement dans l’organisme cible à partir d’un fragment d’ADN intégré artificiellement dans le génome et, donc, un OGM est créé ou 2) pulvérisés depuis l’extérieur et, donc, une nouvelle classe de pesticides aux effets inconnus est créée.
Nucléases à doigts de zinc
TALEN
CRISPR/Cas9
Pour aller plus loin quelques publications ...
Forçage génétique - Gene drive
Gene Drive - Forçage génétique
Qu'est-ce le forçage génétique ?
Le forçage génétique est une application spécifique des nouvelles méthodes de génie génétique. Il s'agit d'une réaction génétique en chaîne qui force la dissémination de gènes modifiés artificiellement en laboratoire dans des populations d'organismes vivant dans la nature. La dissémination dans l'environnement de quelques plantes ou animaux forcés génétiquement suffit à propager les gènes artificiels dans une population entière.
Quels domaines d'application ?




Les chercheurs espèrent utiliser cette technologie pour contrôler génétiquement des organismes sauvages. Les applications du forçage génétique sont conçues en majorité pour exterminer des populations de ravageurs des cultures plutôt que pour assurer la survie d'une espèce - alors que de telles applications sont également concevables avec cette technologie.
Les discussions actuelles ne portent que sur deux applications potentielles : la diminution du nombre d'insectes porteurs de maladies humaines et la protection d'espèces indigènes menacées par des espèces envahissantes agressives. Dans les deux cas, le forçage génétique est présenté comme une approche plus durable et plus sûre pour remplacer les pesticides nocifs et les appâts toxiques. Mais les applications commerciales du forçage génétique dans l'agriculture prévoient d’utiliser cette technologie en complément aux pesticides pour exterminer de nombreux ravageurs agricoles et vaincre la résistance aux herbicides dans des mauvaises herbes courantes. Le forçage génétique est également considéré pour la mise au point d'armes biologiques, un sujet souvent tabou. Jusqu'à présent, les applications du forçage génétique n'ont été testés qu'en laboratoire.
Quels problèmes ?
Contrairement à d'autres manipulations génétiques, où la propagation des caractères artificiellement ajoutés est évitée et indésirable, le forçage génétique a été conçu pour être invasif et irréversible. La mise en circulation de quelques plantes ou animaux dotés d'un gene drive produit artificiellement suffit à déclencher une réaction en chaîne au terme de laquelle tous les membres d'une population portent dans leur génome le trait issu de ce drive. Une fois cette technologie libérée dans l'environnement, il est presque impossible de contrôler ou d'inverser son impact sur l'écosystème. De plus, l'utilisation à grande échelle de cette technologie n'exclut pas une transmission à d'autres espèces sauvages apparentées et représente une menace importante pour la biodiversité avec des effets négatifs considérables sur la santé humaine et environnementale. L'utilisation de cette technologie comme arme biologique représente une menace géopolitique importante. Le forçage génétique nécessite des lignes directrices de recherche qui encouragent une utilisation éthique et responsable. En l'absence d'une réglementation stricte, les organisations nationales et internationales appellent même à un moratoire mondial sur l'utilisation du forçage génétique.
CRISPR/Cas, un élément clé
La technique du forçage génétique consiste à introduire dans le génome d'un organisme une cassette d'ADN qui contient des gènes artificiels choisis par les chercheurs et une boîte d’outils moléculaires, dont les ciseaux moléculaires CRISPR/Cas. Au départ, il faut donc créer un organisme génétiquement modifié, porteur d'une cassette de forçage génétique, puis relâcher cet organisme dans la nature.
C'est cette plante ou cet insecte modifié génétiquement qui se croisera avec des individus sauvages et qui disséminera la cassette de forçage génétique. Et ce sont les ciseaux moléculaires CRISPR/Cas, contenus sur la cassette de forçage génétique, qui permettront la dissémination des gènes artificiels dans les descendants de l'individu porteur. En effet, les ciseaux génétiques CRISPR/Cas9 servent à reconnaître une séquence spécifique du génome et à couper l'ADN à cet endroit précis. À l'endroit de la coupure, les mécanismes naturels de réparation de l'ADN permettent aux gènes artificiels de se copier dans le génome ou de remplacer la version naturelle du gène qui leur ressemblent.
Dans les organismes à reproduction sexuée, chaque descendant contient une copie des chromosomes du père et une copie des chromosomes da la mère. Dans le processus de forçage génétique, on peut dire, en simplifiant, que si le père est porteur de la cassette de forçage génétique, les ciseaux moléculaires CRISPR/Cas permettent aux gènes artificiels de se recopier depuis les chromosomes du père sur les chromosomes de la mère en éliminant toute séquence d'ADN qui leur ressemblent. Ainsi, à chaque nouvelle génération, le génome des descendants du porteur de la cassette de forçage génétique est modifié. Les règles de l'hérédité naturelle dans les organismes à reproduction sexuée sont contournées et la cassette de forçage génétique se propage de génération en génération, éliminant toute séquence d'ADN qui lui ressemble.
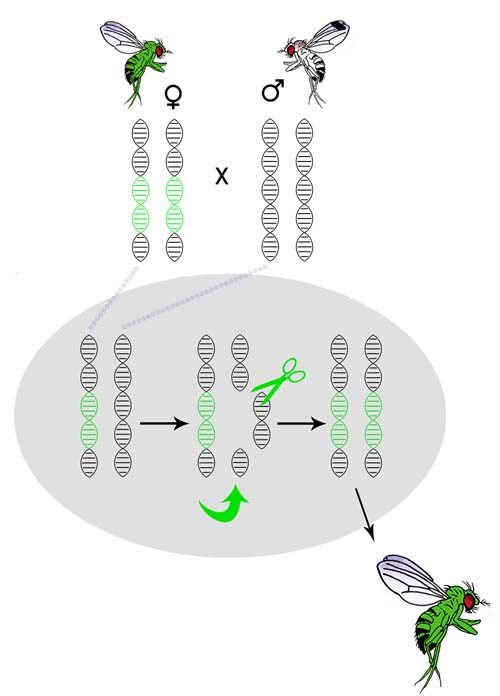
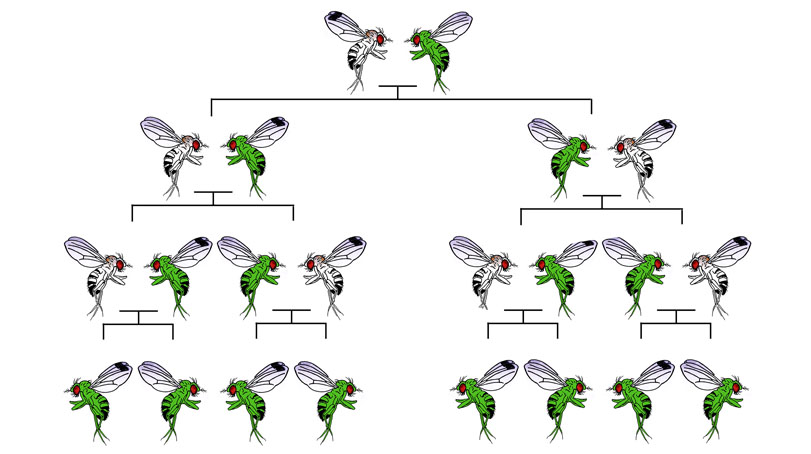
Légende : Les gènes sont transmis à tous les descendants. Normalement, chez la progéniture de ces mouches à fruits, la modification génétique (en vert) ne se situerait que sur le chromosome transmis par la mère. Toutefois, le mécanisme de copie intégré (qui est transmis avec la modification génétique) garantit que cette variante génétique est également copiée dans le chromosome transmis par le père. À la fin du processus, tous les descendants de la paire de mouches à fruits sont homozygotes pour le gène ajouté artificiellement : cela signifie qu'ils portent la même copie du gène sur les deux chromosomes. Comme ce processus se répète à chaque accouplement, après quelques générations, tous les descendants du pedigree sont porteurs de la modification génétique (tous les descendants sont verts).
Conditions relatives à l'application du forçage génétique
Le forçage génétique ne peut se propager avec succès que dans des organismes qui répondent à deux exigences importantes. D'une part, les organismes cibles doivent se reproduire sexuellement afin de permettre la propagation du système de forçage génétique à la descendance de congénères non modifiés. D'autre part, les individus se reproduisent rapidement et le temps entre les générations est court afin que le caractère ajouté artificiellement puisse se répandre rapidement dans toute la population. Les insectes et les rongeurs sont donc très exposés à des manipulations par forçage génétique. L'application du forçage génétique à des plantes à cycle de vie court est peu réaliste car le génome de la plante utilise des mécanismes de réparation de l'ADN qui rendent difficile la transmission de la cassette de forçage génétique (voir "Résistance" ci-dessous).
En outre, certains organismes cibles développent une résistance au forçage génétique. Le mécanisme de forçage génétique, initié par le système CRISPR/Cas, est favorisé par un système de réparation de l'ADN par recombinaison homologue. Certains organismes utilisent d'autres mécanismes de réparation de l'ADN. Ces systèmes de réparation rendent la cassette de forçage illisible ou inactive et bloquent sa propagation de génération en génération.
À peine un an après l’invention du forçage génétique CRISPR, les chercheurs travaillant sur des moustiques édités génétiquement ont également été témoins de l’émergence de résistances au forçage génétique.
Les différents types de forçage génétique
Différents types de cassette de forçage génétique ("gene drive") peuvent être construites selon l'effet théorique souhaité.
Les cassettes de forçage génétique à effet global peuvent être utilisées pour modifier une population (modification/modification/conversion drives) et même la détruire (suppression drives). Ces cassettes de forçage génétique sont conçues de telle sorte que, à l'instar d'une réaction en chaîne inarrêtable, elles se transmettent à l'infini dans la population jusqu'à ce que tous les individus soient modifiés génétiquement, ou jusqu'à ce que la population s'effondre. Ainsi, par exemple, un gène qui confère une résistance à une maladie particulière ou limite la capacité de reproduction de l'espèce peut être disséminé dans toute la population en quelques générations - jusqu'à ce qu'il ne reste plus un seul individu non modifié. Ce type de forçage génétique étant inarrêtable et donc incontrôlable, il peut avoir de graves conséquences.
Diverses techniques sont utilisées pour ralentir et limiter l'effet de ce type de cassettes :
Les Reversal Drives visent bloquer la propagation de la première cassette de forçage génétique par l'introduction d'une deuxième cassette. Un tel mécanisme est peu susceptible de fonctionner de manière fiable en conditions environnementales.
Dans les Split Drives, la cassette de forçage génétique est séparée en deux. Par exemple, une partie du système CRISPR/Cas est localisé sur une première séquence d'ADN. Le reste du système CRISPR/Cas et les gènes artificiels sont situés sur une deuxième séquence. Alors que la première partie de la cassette est incorporé dans l'ADN de l'organisme cible. L'autre partie de la cassette est incorporée dans l'ADN d'un virus qui utilise cet organisme comme hôte. De cette façon, la cassette de forçage génétique n'est complète et ne peut se propager dans l'organisme cible qu'en présence du virus. Cette méthode a été mise au point pour accroître la sécurité en laboratoire. Une application de ce système en conditions environnementales est difficilement réalisable.
Les Daisy Drives ont été mises au point pour s'assurer que le forçage génétique ne fonctionne que localement, au sein d'une population souhaitée et que sa propagation s'arrête au bout d'un certain temps. Dans ce cas, la propagation de la cassette de forçage génétique dépend d'un démarreur, un autre élément d'ADN artificiel inséré dans l'organisme cible. Cet élément n'est pas essentiel pour le fonctionnement de l'organisme cible et tend à disparaître au fil des générations. En l'absence de démarreur, la propagation de la cassette de forçage génétique devrait théoriquement s'arrêter après un certain nombre de générations. Le piège : le démarreur ne doit pas être inactivé par une mutation sinon la propagation de la cassette de forçage génétique est à nouveau inarrêtable.
Liens:
- Video: Gene Drives - Destructifs et incontrôlables
- Rapport complet (2019): Gene Drives
- Video: Gene Drive Moskitos - ein mögliches Zukunftsszenario
